敬告讀者: 《中大通訊》已停刊,本網暫停更新。請移玉步造訪本校最新通訊《走進中大》網頁:https://focus.cuhk.edu.hk,閱讀大學報道和消息。
安內以攘外
鄭詩樂研表觀遺傳治療破肝癌獨有防禦

肝癌是狡猾的殺手,其腫瘤有獨特的防禦能力,能阻止癌症受害者的身體抵抗疾病。不過,鄭詩樂教授的表觀遺傳學研究可能會扭轉乾坤。
肝癌的主要類型是肝細胞癌,構成全球第三大癌症死亡原因。肝癌在東亞地區最普遍,部分原因在於乙型肝炎感染,但由於糖尿病和肥胖症日益增多,西方國家也愈來愈多人罹患肝癌。
免疫療法是現時處理該類型肝癌的治療。藥物包含免疫檢查點抑製劑,可激活殺死癌症的T細胞。由於癌症抑制了這些T細胞,刺激T細胞可以縮小腫瘤,提高患者的存活率。
但是,只有約15%患者對免疫療法有反應。箇中問題在於肝癌是一種「冷」癌,會自行築起壁壘,阻止T細胞進入腫瘤,甚至可以拉攏宿主細胞來抑制T細胞。
鄭教授一直努力探究此防禦機制的運作原理,構思如何突出重圍。他在研究其間發現了表觀遺傳調節劑──稱為「組蛋白脫乙酰基酶8」或「HDAC8」的酶。為了保衞癌細胞,HDAC8會阻止趨化因子的產生,這趨化因子是一種分子信號,可促使T細胞協助身體抵禦癌變。
當他用抑制HDAC8的藥物治療小鼠時,趨化因子以正常方式表達,最終激活T細胞開始浸潤腫瘤。鄭教授將之比喻為「警察最終得以攻入九龍寨城」。九龍寨城曾是香港一座圍城,數十年來一直是法外之境。
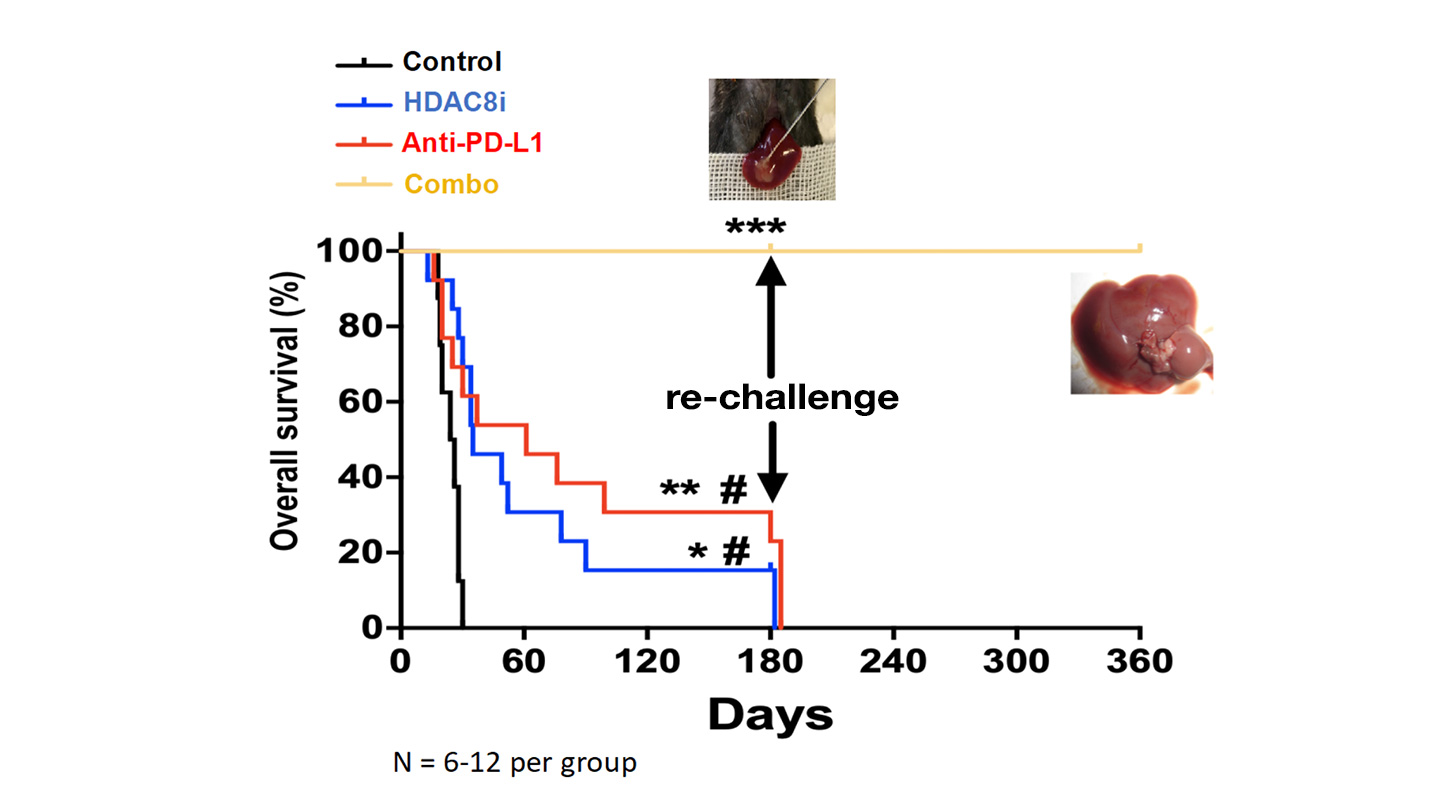
如上圖所示,在實驗室測試中,植入了肝腫瘤的小鼠在未經治療的情況下,會在三十天內死亡。如果單獨使用免疫療法,這些動物的存活期會延長,但全都會在一百八十天內死亡。同樣,接受過表觀遺傳治療的動物會更長壽,但同樣會在一百八十天內死亡。當小鼠同時接受免疫治療以及表觀遺傳治療之後,存活期均超過三百六十天。
「我很詫異,但經反復測試後證實了結果。」鄭教授說:「合併療法的效果很驚人。」
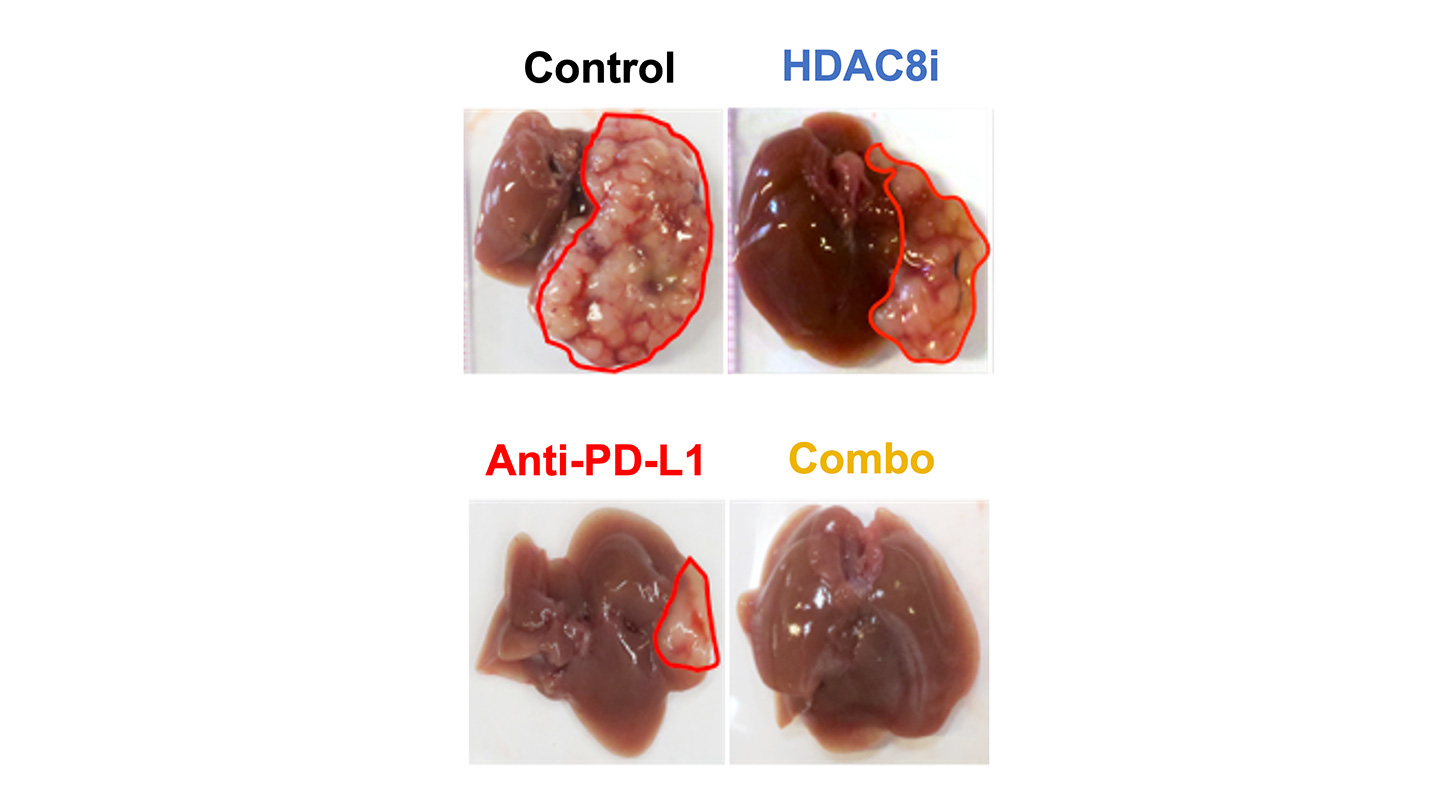
解剖結果(上圖)顯示,當對小鼠只施加一種治療時,癌瘤會縮小,但仍然存在於肝臟中。當小鼠接受免疫治療合併表觀遺傳治療,癌瘤會根除,肝臟完好健康,能自我復原。該發現最近發表於Science Translational Medicine期刊。
鄭教授嘗試在兩種動物模型中找出哪些表觀遺傳基因比較活躍,從中發現到HDAC8的關鍵角色:第一類基因培育的小鼠會變胖而患上肝癌;另一類則因為高脂、高碳水化合物的飲食(相當於餵可口可樂和漢堡包)而患肝癌。
團隊着手研究一百一十五種基因,而HDAC8基因是兩組實驗中唯一「上調」的基因。鄭教授解釋說:「我們發現它確實會大大促進腫瘤增生。」
表觀遺傳學使癌症研究不再拘囿於腫瘤細胞內,得以推展至更廣泛的免疫微環境。遺傳學研究的是固定規律,譬如我們的基因會決定眼睛的顏色;表觀遺傳學領域則研究基因受到外界影響之後的不同表現。
「表觀遺傳學是個全新天地。」鄭教授說:「根據表觀遺傳學,基因表達可以逆轉,缺陷並非永恆。這就是吸引我從事這方面研究的緣由。」
對於其他「冷」或能夠逃脫免疫力攻擊的癌症,包括卵巢癌和胰臟癌,同樣的治療亦可能奏效。
「這些癌症一樣具有高度表達的HDAC8,可導致腫瘤變冷。因此,具針對性的表觀遺傳治療也可能見效。」鄭教授說。
相關的小鼠研究尚未延展至人體臨床試驗。鄭教授現正與德國的藥物開發團隊合作,研發一系列可用作表觀遺傳治療的藥物。鄭教授亦即將與中大藥劑學院的同事測試哪種德國研發的藥物對小鼠最奏效。

如果該藥物配方成效良好,團隊會將它調整至適合人類服用。鄭教授身為中大生物醫學學院腫瘤生物學及實驗藥物治療學主題研究組主管,現正申請該藥劑的研究經費,此過程可能耗時一年左右。
鄭教授估計,如果藥物的安全性和藥效發揮一如理想,可於三年內展開人體試驗。試驗成功後,便可以開始臨床配藥。
大約七成肝癌患者體內都會產生超量的HDAC8。鄭教授說:「研究能為相當多患者帶來好消息。」
新藥將推動精準醫學的前進,醫護人員會根據患者的基因構造和疾病狀況提供個人化治療,畢竟每位病患都情況各異。這樣,他們就不必孤身與病痛作戰了。
中譯/jennylau@cuhkcontents
攝影/Eric Sin
倘中英文版本出現歧義,概以英文版本為準。